Currently this content is only available in English.
Dieser Inhalt ist momentan nur auf Englisch verfügbar.
Die Medgate Kids Line liefert schnell und unkompliziert medizinischen Rat, wenn es Ihrem Kind nicht gut geht. Rund um die Uhr steht Ihnen das medizinische Team unseres Partners Medgate telefonisch zur Verfügung.
0900 712 712 (3.23 CHF / Min.)
nur über private Festnetz- oder Handynummern
0900 712 713 (3.23 CHF / Min.)
für Anrufe von Prepaid-Handys
Für Business-Anschlüsse: 0800 444 333 (Kosten werden über Krankenversicherung abgerechnet)
Bei Notfällen im Ausland rufen Sie die Notfallnummer Ihrer Krankenkasse an. Diese finden Sie jeweils auf Ihrer Krankenkassenkarte.
Notfallnummern
Beratungstelefon für Kinder- und Jugendnotfälle
Die Medgate Kids Line liefert schnell und unkompliziert medizinischen Rat, wenn es Ihrem Kind nicht gut geht. Rund um die Uhr steht Ihnen das medizinische Team unseres Partners Medgate telefonisch zur Verfügung.
0900 712 712 (3.23 CHF / Min.)
Festnetz und Handy-Abo
0900 712 713 (3.23 CHF / Min.)
Prepaid-Handys
Für Business-Anschlüsse: 0800 444 333 (Kosten werden über Krankenversicherung abgerechnet)
Für Notfälle im Ausland: Rufen Sie die Notfallnummer Ihrer Krankenkasse an. Diese finden Sie jeweils auf Ihrer Krankenkassenkarte.
Wichtige Notfallnummern
- 144 Ambulanz
- 145 Tox Info Suisse (Vergiftungen)
- 117 Polizei
- 118 Feuerwehr
Kontakt Box
Kontakt
Zu welchem Thema möchten Sie uns kontaktieren?
Für Lob oder Tadel nutzen Sie bitte das Feedback-Formular.
Terminvereinbarung sind nicht über das Kontaktformular möglich. Für Terminvereinbarungen und -verschiebungen wenden Sie sich bitte an die Leitstelle Poliklinik +41 61 704 12 20
Mahnung / Inkasso
Patientenabrechnung
Bitte kontaktieren Sie mich
Sonstiges
Wirbelsäule und Rückenmark
Hier stellen wir Ihnen eine kleine Auswahl typischer Krankheitsbilder vor, welche die Pädiatrische Neurochirurgie am UKBB mit modernsten Methoden behandelt.
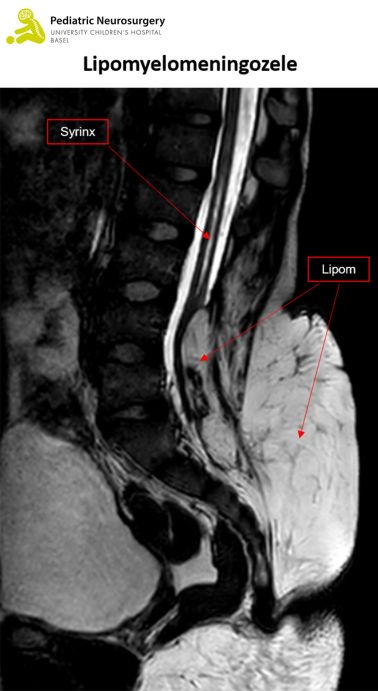
Lipomyelomeningocele
Die wichtigsten Punkte
- Eine Lipomyelomeningocele ist eine Verschlusserkrankung der Wirbelsäule.
- Fettgewebe wächst in das Rückenmark hinein und führt zu einer Anhaftung (tethering) des Rückenmarks.
- Symptome können erst spät auftreten, klassischerweise zeigt sich eine Beule unter der Haut.
- Bei der Operation wird das Fettgewebe entfernt und das angehaftete Rückenmark gelöst.
- Die Prognose ist insgesamt sehr gut.
- Der neurologische Outcome ist von der Grunderkrankung abhängig.
Diagnose, Behandlung und Prognosen
Krankheitsbild
Was ist eine Lipomyelomeningocele?
Die Lipomyelomeningocele ist eine Form der geschlossenen Fehlbildung des Wirbelkanals (sogenannte okkulte Spina bifida oder geschlossene Dysraphie). Im Vergleich zu den geschlossenen Dysraphien, wo die Haut über der Fehlbildung verschlossen ist, spricht man von einer offenen Dysraphie (auch Spina bifida aperta oder Myelomeningocele genannt) wenn die Haut am Rücken offen ist und das Rückenmark und die Nerven freiliegen. Im Falle einer Lipomyelomeningocele verschliesst sich der Wirbelknochen und die Hirnhaut während der embryonalen Entwicklung (während der Schwangerschaft) nicht und eine Fettwucherung (sogenanntes Lipom) der Unterhaut führt zu Verklebungen und Verwachsungen des Rückenmarks mit den Nerven und der Umgebung. Dies führt zu einem Zug am Rückenmark (sogenanntes tethered cord) was zu neurologischen Ausfälle führen kann. Die Lipomyelomeningocele ist die häufigste Form einer okkulten Dysraphie. Lipome im Rückenmark, so wie die Lipomyelomeningocele, kommen in ca.1 auf 4000 Lebendgeburten vor, wobei die Lipomyelomeningocele ca. 80% der Fälle ausmacht. Die Ursache einer Lipomyelomeningocele ist unbekannt. Risikofaktoren, die mit der Lipomyelomeningocele vergesellschaftet sind schlecht kontrollierter Schwangerschaftsdiabetes, Übergewicht der Mutter und gewisse Medikamente (vor allem Antiepileptika) zu einer Lipomyelomeningocele führen.
Symptome
Was sind typische Zeichen einer Lipomyelomeningocele?
Typische Zeichen der Lipomyelomeningocele sind eine weiche, schmerzlose Hautbeule am Rücken. Weitere Veränderungen der Haut, die im Zusammenhang mit einer Lipomyelomeningocele vorkommen können sind z.B. eine Asymmetrie des Hinterns (sogenannte «gluteal fold deviation»), eine rötliche Verfärbung der Haut (sogenanntes «Hämangiom»), ein vermehrtes Haarwachstum im Bereich der Beule, oder eine Eindellung im Bereich des Steissbeins (sogenanntes «non-simple dimple»). In der Regel weisen Babys noch keine neurologischen Symptome auf. Mit dem Alter können jedoch neurologische Symptome auftreten, unter anderem Ausfälle der Blasen und Darmfunktion (Inkontinenz und/oder Verstopfung), Kraft und Empfindungsstörungen, Ausfall oder Steigerung der Reflexe und Probleme der Beine (offene Hautstellen, Klumpfüsse, Hüftluxationen etc.). Ältere Kinder können häufiger auch Schmerzen haben, diese sind auf den unteren Rücken beschränkt und verstärken sich bei allen Bewegungen, die den Rücken (und damit das Rückenmark) dehnen.
Diagnose
Wie wird eine Lipomyelomeningocele diagnostiziert?
In der Regel fällt eine Lipomyelomeningocele bereits bei der Geburt durch die oben beschriebenen Hautzeichen auf. Häufig wird der Verdacht mittels Ultraschall bestätigt. Danach sollte eine Magnet Resonanz Tomographie (MRT) des Rückens gemacht werden um das genaue Ausmass der Lipomyelomeningocele zu erfassen und die Behandlung planen zu können.
Therapie
Wie lässt sich eine Lipomyelomeningocele behandeln?
Die operative Entfernung des Lipoms und Entlastung der Nerven und des Rückenmarks ist die Therapie der Wahl um neurologische Ausfälle zu verhindern oder einzuschränken. Diese Operation wird prophylaktisch durchgeführt idealerweise im Alter von 6-9 Monaten, also noch bevor man weiss, ob neurologische Symptome bestehen. Ziel der Operation ist möglichst früh das Rückenmark zu entlasten damit keine neurologischen Symptome entstehen, respektive falls Symptome schon vorhanden sind, dass diese nicht voranschreiten. Dabei wird der Rücken des Kindes eröffnet und das Lipom im Rückenmark vorsichtig entfernt, dafür werden meistens, zusätzlich zu den schon durch die Erkrankung offenen Wirbelköper, 1-2 weitere Wirbelkörper eröffnet. Das Rückenmark wird entlastet (sogenanntes «untethering») damit kein Zug mehr auf das Rückenmark besteht. Anschliessend wird das Rückenmark wieder verschlossen und die darüber liegende Hirnhaut, Muskeln und Haut werden zugenäht. Die Operation wird mit einem sogenannten Neuromonitoring durchgeführt, das heisst, dass die Aktivitäten der Nerven aufgezeichnet werden und der Chirurg somit weiss wo er sich befindet und welche Strukturen geschützt werden müssen. Bei diesen Operationen kommt es selten zu Komplikationen. Es kann unter anderem zu einem Loch in der Hirnhaut kommen, durch den Hirnwasser austritt, zu Wundinfekten und in ganz seltenen Fällen zu neuen neurologischen Ausfällen (1%). In seltenen Fällen kann es nach der Operation zu einem sogenannten «re-tethering» kommen, einer erneuten Verwachsung des Rückenmarks mit einem Rezidiv (Rückfall oder erneutes Wachstum) des Lipoms oder mit dem Narbengewebe. Dies kann wiederum mit neurologischen Ausfälle wie Verlust der Blasenfunktion, Fehlstellungen des Rückens oder der Extremitäten und Schmerzen verbunden sein. Eine weitere Operation (re-untethering) ist nur indiziert falls eine neurologische Verschlechterung objektivierbar ist.
Spitalaufenthalt
Wie läuft der Spitalaufenthalt meines Kindes ab?
Während des gesamten Spitalaufenthaltes wird Ihr Kind von unserem Team der pädiatrischen Neurochirurgie im UKBB betreut. Ihr Kind tritt einen Tag vor der Operation ein, wird durch unser Team und die Narkoseärzte (Anästhesie) nochmals untersucht und kann dann, falls Sie dies wünschen, zuhause schlafen. Am nächsten Tag wird Ihr Kind operiert und kommt anschliessend zur Überwachung auf die Intensivpflegestation. Am Operationstag steht Ihnen eine unserer Elternbegleiterinnen vom Eltern Begleitungsservice (BELOP) am UKBB zur Verfügung. Sie begleiten die Sie, bis ihr Kind eingeschlafen ist und zeigen Ihnen, wo ihr Kind wieder aufwachen wird. Zwischendurch helfen sie Ihnen, sich im Spital zurechtzufinden. Sobald Ihr Kind keine engmaschige Überwachung mehr braucht (in der Regel am Folgetag), kommt es auf die kinderchirurgische Bettenstation. Um das Risiko für Hirnwasser-Lecks möglichst zu minimieren wird Ihr Kind für die ersten 48 Stunden nach der Operation möglichst flachliegen, danach kann es sofort wieder vollständig mobilisiert werden. In der Regel erholt sich Ihr Kind nach 5-7 Tagen von der Operation und darf auch in diesem Zeitraum nach Hause austreten. Während der gesamten Zeit dürfen Sie bei Ihrem Kind sein und sich mit Fragen an das Team der pädiatrischen Neurochirurgie wenden, welches täglich zur Visite bei Ihnen und Ihrem Kind vorbeikommt.
Prognose
Welche Prognose hat eine Lipomyelomeningocele?
Die Prognose bei Kindern mit einer Lipomyelomeningocele ist in der Regel sehr gut, hängt jedoch mit den Symptomen und Einschränkungen zusammen (Rückendeformitäten, Blasenfunktionsstörungen) die damit auftreten. Die Kinder haben eine normale Intelligenz, und oft eine sehr gute Lebensqualität. Gewisse Kinder zeigen trotz Behandlung Blasen- und/oder Mastdarm Funktionsstörungen, Rückenschmerzen, Skoliose und andere neurologische Ausfälle. Das Lipom ist eine niedriggradige Läsion und ist nicht lebensgefährlich. Die operierten Kinder werden jährlich über Jahre in unsere interdisziplinäre Sprechstunde am UKBB von mehreren Spezialisten (Kinderneurochirurgen, Kinderneurologen, Kinderurologen und Kinder-Neuroorthopäden) betreut und versorgt.
Literatur
Weiterführende Literatur
Stricker S, Eberhardt N, Licci M, Greuter L, Raphael G, Soleman J. Wound closure with a mesh and liquid tissue adhesive (Dermabond Prineo) system in pediatric spine surgery: a prospective single-center cohort study incorporating parent-reported outcome measures. J Neurosurg Pediatr. Sept 2022. doi.org/10.3171/2022.8.PEDS22270
Myelomeningocele (Offener Rücken)
Die wichtigsten Punkte
- Die Myelomeningocele ist eine angeborene Erkrankung mit fehlender Verschluss des Rückens und freiliegendem Rückenmark
- Oft wird die Diagnose schon in der Schwangerschaft im Ultraschall gestellt
- Bei einer Operation werden die Nervenstruckturen rekonstruiert und der Rücken verschlossen
- Die Prognose ist abhängig von der Höhe der Myelomeningocele und den Begleiterscheinungen
Diagnose, Behandlung und Prognosen
Krankheitsbild
Was ist ein offener Rücken?
Neuralrohrdefekte, die zu einem sogenannten offenen Rücken («Spina bifida») führen, gehören zu den häufigsten angeborenen Krankheiten. Die Myelomeningocele ist die häufigste Form eines offenen Rückens und beschreibt eine offene Spalte in der Wirbelsäule mit einem begleitenden Hautdefekt darüber, durch den die Hirnhäute und das Rückenmark gesehen werden bzw. herauskommen können. Dies kommt aufgrund eines fehlenden/eingeschränkten Verschlusses der Nervenplatte während der sogenannten Neurulation, der Bildung unseres Nervensystems inklusive Gehirn und Rückenmark, während der frühen Entwicklung zustande. Dies führt dann wiederum zu dem Defekt in der Wirbelsäule und des Rückenmarks, der dann als offener Rücken sichtbar ist. Eine Myelomenigocele kommt zwischen 1-7 pro 1000 Geburten vor und kann aufgrund von verschiedensten Faktoren (einzeln oder kombiniert) auftreten. Einer der bekanntesten Risikofaktoren für einen offenen Rücken ist ein Folsäure-Mangel, weiterhin können genetische Faktoren (wobei eine familiäre Häufung erkennbar ist, ca. 2% Wiederholungsrate), ein weibliches Geschlecht, schlecht kontrollierter Schwangerschaftsdiabetes, Übergewicht der Mutter, gewisse Medikamente (vor allem Antiepileptika), Exposition zu Pestiziden oder aber auch verschiedene Syndrome (Trisomie 13 & 18, Meckel-Gruber Syndrom, Roberts-Syndrom, Jarcho-Levin Syndrom, HARD- Syndrom) zu einer Myelomeningocele führen.
Symptome
Was sind typische Zeichen eines offenen Rückens?
Ein offener Rücken wird heutzutage normalerweise in Vorsorgeuntersuchungen während der Schwangerschaft festgestellt. Dies wird normalerweise im Rahmen der Standard-Vorsorgeuntersuchung mittels Ultraschall festgestellt. Zusätzlich wird der Folsäurespiegel gemessen und bei einem erhöhten Verdacht wird das alpha-feto Protein (AFP) im mütterlichen Blut untersucht. Diese Kombination ermöglicht eine relativ sichere Detektion einer Myelomeningocele. Selten wird es erst bei der Geburt entdeckt. Kinder mit einer Myelomeningocele zeigen bei der Geburt einen offenen Rücken, bei dem die beiden Nervenplatten und oftmals ein Sack, der aus dem Rücken austritt und die Hirnhäute und Hirnwasser enthält, zu sehen sind. Dieser Defekt tritt vor allem in den unteren Anteilen der Wirbelsäule auf, kann aber theoretisch auf jeder Höhe der Wirbelsäule vorkommen. Durch die Freilegung des Rückenmarks kann es zu neurologischen Ausfällen sowohl der Muskulatur und der Gefühlsempfindung aber auch der autonomen Funktionen wie zum Beispiel einem Verlust der Blasen- und der Mastdarmkontrolle kommen. Schliesslich kann es im Rahmen einer Myelomeningocele in ca. 50-60% der Fälle, zu einem Wasserkopf («Hydrocephalus») und den damit verbundenen Problemen kommen (siehe Factsheet «Hydrocephalus»). Zusätzlich zeigen praktisch alle Kinder mit einer Myelomeningocele ein sogenannte Chiari II Malformation, einen Tiefstand der Kleinhirnmandeln (sogenannte Tonsillen), die jedoch nur selten eine Behandlung bedarf.
Diagnose
Welche weiterführende Diagnostik ist bei Verdacht eines offenen Rückens notwendig?
Ein offener Rücken wird in der Regel in Vorsorgeuntersuchungen während der Schwangerschaft festgestellt. Dies wird im Rahmen der Standard-Vorsorgeuntersuchung mittels Ultraschall festgestellt. Zusätzlich wird der Folsäurespiegel gemessen und bei einem erhöhten Verdacht wird das alpha-feto Protein (AFP) im mütterlichen Blut untersucht. Diese Kombination ermöglicht eine relativ sichere Detektion für einen Verdacht auf eine Myelomeningocele. Im Falle eines auffälligen Schwangerschaftsscreenings werden oftmals weitere genetische Untersuchungen (z.B. die Suche nach weiteren Anomalien etc.) sowie ein MRI durchgeführt.
Im seltenen Fall, bei dem ein offener Rücken nicht während der Schwangerschaftsvorsorgeuntersuchung entdeckt wird, zeigen sich bei Geburt die oben beschriebenen charakteristischen Zeichen, welche die Diagnose ermöglichen.
Therapie
Wie lässt sich ein offener Rücken behandeln?
Alle Kinder welche mit einem offenen Rücken geboren werden, müssen innerhalb von 24-48 Stunden operiert werden. In der Regel wird eine Meningomyelocele schon während der Schwangerschaft festgestellt und ein Beratungsteam aus verschiedenen Fachdisziplinen kann mit Ihnen die jeweiligen Optionen genauestens besprechen. Prinzipiell besteht ebenfalls die Option, eine Operation im Mutterleib durchzuführen (sogenannte fetale Operation). Das ist eine Operation, bei der die Gebärmutter eröffnet wird und dann im Mutterleib selbst operiert wird. Dies hat eine leichtgradige Verbesserung der Entwicklung sowie eine geringere Rate an Hydrocephalus zur Folge, zeigt aber nur eine leichte Verbesserung der Lebensqualität. Zusätzlich kommen die mütterlichen Risiken der Operation dazu, welche unter anderem aus Frühgeburtlichkeit, Plazentaablösungen und Entzündungen der Eihaut (Chorioamnionitis) bestehen. Wir am UKBB wenden die Operation bei lebendgeborenen Kindern an. Dabei wird direkt nach der Geburt eine neurologische Untersuchung durchgeführt, die den Ausmass der neurologischen Einschränkungen des Kindes erfasst. Anschliessend wird der offene Rücken innerhalb der ersten 24-48 Lebensstunden chirurgisch verschlossen. Zusätzlich erhalten die Kinder eine antibiotische Therapie, um eine Infektion im Zentralnervensystem zu verhindern. Das Kind wird dafür unter Narkose auf dem Bauch gelagert und der Rücken vorsichtig eröffnet. Die jeweiligen Schichten der Muskulatur, des Rückenmarks, der Dura (Hirnhaut) und der Rückenhaut werden rekonstruiert und zusammengefügt. Anschliessend wird der Rücken wieder verschlossen. Falls ein Hydrocephalus vorliegen sollte, wird dieser ebenfalls behandelt, weitere Informationen dazu finden Sie auf unserer Website unter «Hydrocephalus».
Spitalaufenthalt
Wie läuft der Spitalaufenthalt meines Kindes ab?
Während des gesamten Spitalaufenthaltes wird Ihr Kind von unserem Team der pädiatrischen Neurochirurgie im UKBB betreutt. Nach der Geburt wird Ihr Kind auf der Neugeborenen-Intensivstation überwacht, mit Antibiotika gegen mögliche Infektion versorgt und dann in der Regel innerhalb von einem Tagen neurochirurgisch versorgt. Am Operationstag steht Ihnen eine unserer Elternbegleiterinnen vom Eltern Begleitungsservice (BELOP) am UKBB zur Verfügung. Sie begleiten die Eltern, bis das Kind eingeschlafen ist und zeigen den Eltern, wo es wieder aufwachen wird. Zwischendurch helfen sie Ihnen, sich im Spital zurechtzufinden. Nach der Operation kommt Ihr Kind zur Überwachung zurück auf die Neugeborenen-Intensivstation. Sobald Ihr Kind keine engmaschige Überwachung mehr braucht, kommt es auf die Mutter-Kind Abteilung. Sobald Ihr Kind sich von der Operation erholt hat, darf es mit Ihnen nach Hause. Während der gesamten Zeit dürfen Sie bei Ihrem Kind sein und sich mit Fragen an das Team der pädiatrischen Neurochirurgie wenden..
Prognose
Welche Prognose hat eine behandelte Myelomeningocele?
Kinder mit einer Myelomeningocele haben eine gute Lebenserwartung, die geistige und körperliche Entwicklung ist jedoch stark abhängig von der Höhe der Myelomeningocele und den Begleiterscheinungen (zum Beispiel Wasserkopf, Rückendeformitäten, Blasenfunktionsstörungen). Die meisten Kinder haben eine normale Intelligenz, können jedoch Lernschwächen zeigen. Gewisse Kinder können laufen andere sind Rollstuhlgängig. Blasen- und Mastdarmstörungen sind in bis zu 60% der betroffenen Kinder vorhandenn, wobei gewisse Kinder mit Myelomeningocele auch eine normale Funktion aufzeigen können. Ca. 10-25% der Kinder mit einer Myelomeningocele entwickeln epileptische Anfälle im Laufe der Zeit, dies kann auch in Zusammenhang mit ei einem Hydrocephalus im Rahmen der Myelomeningocele vorkommen. Leider kann man den Schweregrad der neurologischen und kognitiven Einschränkungen vor der Geburt nur sehr schlecht einschätzen. Rückenprobleme im Sinne einer Skoliose (Schiefer Rücken) oder Tethered cord (Anhaften des Rückenmarks) können ebenfalls vorkommen und könnten zu weiteren Operationen führen im Sinne einer Skoliose Operation (Aufrichtungs-Operation) oder einer Untethering Operation (Loslösung des Rückenmarks) worauf sich die Beschwerden in der Regel rasch bessern. Alle Kinder mit behandelter Myelomeningocele werden über die Jahre in unsere interdisziplinäre Myelomeningocele Sprechstunde am UKBB regelmässig nachkontrolliert. Im Rahmen dieser Sprechstunde wird Ihr Kind von unserem Team der pädiatrischen Neurochirurgie gesehen sowie von den Kinderneurologen und bei Bedarf den Kinderurologen, Kinderorthopäden, Kindernephrologen und unserem Sozialdienst.
Literatur
Weiterführende Literatur
Licci M, Guzman R, Soleman J. Maternal and obstetric complications in fetal surgery for prenatal myelomeningocele repair: a systematic review. Neurosurg Focus. 2019;47(4):E11. doi:10.3171/2019.7.FOCUS19470
Stricker S, Balmer C, Guzman R, Soleman J. Dizygotic opposite-sex twins with surgically repaired concordant myelomeningocele conceived by in vitro fertilization using intracytoplasmic sperm injection: a case report and review of the literature. Child’s Nerv Syst ChNS Off J Int Soc Pediatr Neurosurg. 2019;35(4):725-728. doi:10.1007/s00381-018-3990-8
Licci M, Zaed I, Beuriat PA, Szathmari A, Guibaud L, Mottolese C, Di Rocco F. CSF shunting in myelomeningocele-related hydrocephalus and the role of prenatal imaging. Child’s Nerv Syst ChNS Off J Int Soc Pediatr Neurosurg. 2021;37(11):3417-3428. doi:10.1007/s00381-021-05217-5
Mitra SS, Feroze AH, Gholamin S, Richard C, Esparza R, Zhang M, Azad TD, Alrfaei B, Kahn SA, Hutter G, Guzman R, Creasey GH, Plant GW, Weissman IL, Edwards MS, Cheshier S. Neural Placode Tissue Derived From Myelomeningocele Repair Serves as a Viable Source of Oligodendrocyte Progenitor Cells. Neurosurgery. 2015;77(5):794-802; discussion 802. doi:10.1227/NEU.0000000000000918
Stricker S, Eberhardt N, Licci M, Greuter L, Raphael G, Soleman J. Wound closure with a mesh and liquid tissue adhesive (Dermabond Prineo) system in pediatric spine surgery: a prospective single-center cohort study incorporating parent-reported outcome measures. J Neurosurg Pediatr. Sept 2022. doi.org/10.3171/2022.8.PEDS22270
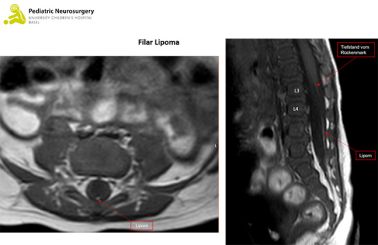
Filum terminale Lipom
Die wichtigsten Punkte
- Ein Filum terminale Lipom ist eine minimale Ansammlung von Fettgewebe am unteren Ende des Rückenmarks.
- Diese führt meistens zu einer Elastizitätsverlust des Rückenmarks und somit zu Zug auf die Nerven (tethered cord syndrome)
- Die meisten Fälle zeigen keine Symptome und Symptome können erst spät auftreten.
- Bei der wird das Filum mit dem Fettgewebe durchtrennt damit kein Zug mehr vorhanden ist auf das Rückenmark (untethering)
- Die Prognose ist exzellent und abhängig von den Begleiterkrankungen
Diagnose, Behandlung und Prognosen
Krankheitsbild
Was ist ein Filum terminale Lipom (FTL)?
Das Filum terminale ist ein bindegewebiges Band, dass das Ende des Rückenmarks (sogenannter Conus) mit dem Hirnhautsack, der das Rückenmark beinhaltet, und dem Steissbein verbindet und somit eine Zuggurtung für das Rückenmark macht. Bei einem FTL findet eine «Verfettung» dieses Bandes statt, und die Dehnbarkeit wird eingeschränkt was zu einem stärkeren Herunterziehen des Rückenmarks führen kann (sogenanntes tethered cord syndrome), was wiederum zu neurologischen Problemen führen kann. Das FTL ist neben der Lipomyelomeningocele die häufigsten Formen einer okkulten spinalen Dysraphie (eine Form des offenen Rückens). Beide Formen, kommen in ca. 1 auf 4000 Lebendgeburten vor, wobei die Lipomyelomeningocele die häufigste Form des Lipoms (ca. 80%) ist und das FTL etwa 10% der Fälle ausmacht. Mädchen sind häufiger betroffen als Jungs. Ursächlich ist wie beim offenen Rücken ein Fehler bei der Entwicklung des Nervensystems, bei dem wahrscheinlich embryonale Zellen nicht richtig funktioniert haben und es zu einem Defekt im Rückenmark kommt, durch den wiederum Fettzellen einwandern und sich ausbreiten können. Die genaue Ursache ist jedoch bisher unklar. Ein FTL kann im Rahmen von seltenen Syndromen wie dem VACTERL und Currarino Syndrom auftreten.
Symptome
Was sind typische Zeichen eines FTL?
Oft wird man auf ein FTL durch typischen Hautzeichen wie ein behaartes Gebiet am Rücken (sogenannte «Hypertrichose»), eine rötliche Verfärbung (sogenanntes «Hämangiom»), eine kleine Eindellung in der Haut am Rücken (sogenannter «non-simple dimple»), oder eine Abweichung der Falte im Bereich des Pos («gluteal fold deviation») aufmerksam. Selten werden FTLs zufällig bei einer Bildgebung des Rückens gefunden. Die meisten früh (vor dem 6. Lebensmonat) detektierten FTLs sind asymptomatisch, jedoch können betroffene Kinder in ca. 30% der Fälle mit dem Alter Symptome wie Ausfälle der Blasen (ca. die Hälfte der Patienten ist davon betroffen) und Darmfunktion (Inkontinenz und/oder Verstopfung), Kraft und Empfindungsstörungen (ca. 15%), Ausfall oder Steigerung der Reflexe und Probleme der Beine (offene Hautstellen, Klumpfüsse, Hüftluxationen etc., ca. 30%) entwickeln. Ältere Kinder können häufiger auch Schmerzen haben, diese sind auf den unteren Rücken beschränkt und verstärken sich bei allen Bewegungen, die den Rücken (und damit das Rückenmark) dehnen.
Diagnose
Welche weiterführende Diagnostik ist bei Verdacht auf ein FTL notwendig?
Ein FTL wird oftmals per Zufall bemerkt, unter anderem durch die oben erwähnten Hautmerkmale, da es meist keine Beschwerden verursacht. Ein Ultraschall (nur im Säuglingsalter möglich) stellt die primäre Untersuchungsmethode dar, kann aber oft ein FTL nicht komplett ausschliessen, weswegen eine Magnet Resonanz Tomographie (MRT) des Rückens gemacht wird um die Diagnose zu bestätigen. Zusätzlich dient das MRT zur Indikationsstellung der Operation, dabei spricht ein sogenannter tiefliegender Conus (zu tiefliegendes Rückenmarksende, unterhalb des 3. Wirbelknochens) für einen Zug auf das Rückenmark (tethered cord syndrome), was in der Regel zur Empfehlung der Operation führt.
Therapie
Wie lässt sich ein FTL behandeln?
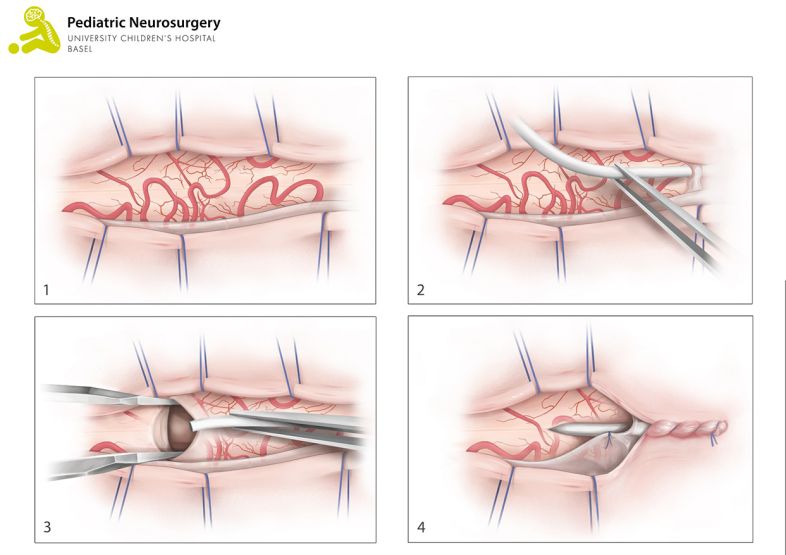
Falls ein FTL diagnostiziert wurde, sollte eine Operation erfolgen um spätere Symptome zu verhindern. Bei der Operation wir der Rücken des Kindes eröffnet. Am UKBB wählen wir einen minimal invasiven Eingriff bei dem die knöchernen Wirbelstrukturen möglichst geschont werden und praktisch nur Muskeln und Bänder eröffnet werden. Der Hautschnitt dafür ist etwa 3 cm lang. Nach Eröffnung der Muskulatur, Knochen und Bänder wird die Hirnhaut eröffnet und das FTL aufgesucht. Die Operation wird mit sogenanntem Neuromonitoring durchgeführt, das heisst, dass die Aktivitäten der Nerven aufgezeichnet werden und der Chirurg somit weiss, wo er sich befindet und welche Strukturen geschützt werden müssen. Das FTL wird dabei mit Strom stimuliert und da es keine neurologische Aktivität im Bereich des Filums gibt, sollte die Messung negativ ausfallen und das Filum kann durchgeschnitten werden. Die Operation dauert ca. 3-4 Stunden. Bei diesen Operationen kommt es selten zu Komplikationen. Es kann unter anderem zu einem Leck kommen, durch dem Hirnwasser austritt, zu Wundinfekten und in ganz seltenen Fällen zu neuen neurologischen Ausfällen (in 0-1% der Fälle). In sehr seltenen Fällen kann es nach der Operation zu einem sogenannten «re-tethered cord» kommen, ein Rückfall durch Verwachsung des Filums mit der Operationsnarbe. Dies führt zu einer erneuten Dehnung des Rückenmarks und kann mit Verlust der Blasenfunktion, Fehlstellungen des Rückens und Schmerzen verbunden sein. Das re-tethering wird durch eine weitere Operation von der Narbe abgelöst, worauf sich die Beschwerden in der Regel rasch bessern.
Spitalaufenthalt
Wie läuft der Spitalaufenthalt meines Kindes ab?
Während des gesamten Spitalaufenthaltes wird Ihr Kind von unserem Team
der pädiatrischen Neurochirurgie im UKBB betreut. Ihr Kind tritt einen Tag vor
der Operation ein, wird durch unser Team und die Narkoseärzte (Anästhesie)
nochmals untersucht und kann dann, falls Sie dies wünschen, zuhause schlafen.
Am nächsten Tag wird Ihr Kind operiert und kommt anschliessend zur Überwachung
auf die Intensivpflegestation. Am Operationstag steht Ihnen eine unserer
Elternbegleiterinnen vom Eltern Begleitungsservice (BELOP) am UKBB zur
Verfügung. Sie begleiten die Eltern, bis das Kind eingeschlafen ist und zeigen
den Eltern, wo es wieder aufwachen wird. Zwischendurch helfen sie Ihnen, sich
im Spital zurechtzufinden.
Sobald Ihr Kind keine engmaschige Überwachung mehr
braucht (in der Regel am Folgetag), kommt es auf die kinderchirurgische
Bettenstation. Um das Risiko für Hirnwasser-Lecks möglichst zu minimieren wird
Ihr Kind für die ersten 48 Stunden nach der Operation möglichst flachliegen,
danach kann es sofort wieder vollständig mobilisiert werden. In der Regel
erholt sich Ihr Kind nach 3-5 Tagen von der Operation und darf auch in diesem
Zeitraum nach Hause austreten.
Während der gesamten Zeit dürfen Sie bei Ihrem
Kind sein und sich mit Fragen an das Team der pädiatrischen Neurochirurgie
wenden, welches täglich zur Visite bei Ihnen und Ihrem Kind vorbeikommt.
Prognose
Welche Prognose hat eine behandelte Kraniosynostose?
Die Prognose bei Kindern mit einem FTL ist exzellent, wenn die Operation frühzeitig (im Alter von 6-9 Monate) durchgeführt wird. Die operierten Kinder werden über ein bis zwei Jahre in unserer Sprechstunde nachkontrolliert, danach erfolgen die gewöhnliche kinderärztliche Kontrollen.
Literatur
Weiterführende Literatur
Lalgudi Srinivasan H, Valdes-Barrera P, Agur A, Soleman J et al. Filum terminale lipomas-the role of intraoperative neuromonitoring. Child’s Nerv Syst ChNS Off J Int Soc Pediatr Neurosurg. 2021;37(3):931-939. doi:10.1007/s00381-020-04856-4
Greuter L, Licci M, Terrier A, Guzman R, Soleman J. Minimal invasive interlaminar approach for untethering of fatty filum terminale in pediatric patients — how I do it. Acta Neurochir (Wien). Published online 2022. doi:10.1007/s00701-022-05204-y
Lalgudi Srinivasan H, Valdes-Barrera P, Agur A, Soleman J, Ekstein M, Korn A, Vendrov I, Roth J, Constantini S. Filum terminale lipomas-the role of intraoperative neuromonitoring. Childs Nerv Syst. 2021 Mar ;37(3):931-939. doi: 10.1007/s00381-020-04856-4.
Stricker S, Eberhardt N, Licci M, Greuter L, Raphael G, Soleman J. Wound closure with a mesh and liquid tissue adhesive (Dermabond Prineo) system in pediatric spine surgery: a prospective single-center cohort study incorporating parent-reported outcome measures. J Neurosurg Pediatr. Sept 2022. doi.org/10.3171/2022.8.PEDS22270
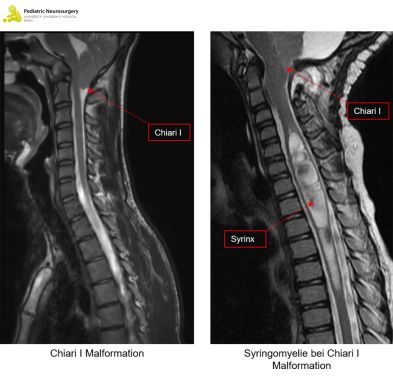
Chiari Malformation Typ I und Syringomyelie
Die wichtigsten Punkte
- Als Chiari Malformation Typ I (CMI) werden relativ seltene Fehlbildungen im hinteren Bereich des Kopfes und am Übergang zum Rückenmark bezeichnet. Eine Syringomyelie beschreibt einen flüssigkeitsgefüllten Hohlraum im Rückenmark und tritt oft zusammen mit einer CMI auf.
- Eine CMI ist meistens angeboren, aber nicht vererbt. Die genaue Entstehung ist nicht geklärt.
- 90 Prozent der CMI-Fälle sind Zufallsbefunde, bei denen keine Symptome auftreten und auch keine Therapien notwendig sind.
- Auftretende Symptome infolge einer CMI können wenig bis schwerstgradig einschränkend sein. Sie lassen sich chirurgisch behandeln und führen bei rund 80 Prozent der Patient*innen zu einer Verbesserung. Ähnlich verhält es sich mit Symptomen und Behandlung einer Syringomyelie.
- Die Prognose hängt von den Symptomen und Schweregrad der Syringomyelie ab.
Diagnose, Behandlung und Prognosen
Krankheitsbild
Was ist eine Chiari Malformationen Typ I (CMI)?
Die Chiari Malformationen Typ I (CMI) ist eine meistens angeborene strukturelle Anomalie im Bereich des Kleinhirns, Hirnstamms und am Übergang zum Rückenmark. Dabei liegen die sogenannten Kleinhirnmandeln oder Kleinhirntonsillen entweder mit oder ohne Hirnstamm mehr als fünf Millimeter tief im Rückenmarkskanal (sogenannte Kleinhirntonsillen-Ektopie).
Eine CMI kommt bei etwa 1 bis 3 Prozent der Gesamtbevölkerung vor und ist somit relativ selten.
Nur in 10 Prozent der Fälle treten Symptome auf, die eine Behandlung erfordern. 90 Prozent der CMI-Fälle sind Zufallsbefunde und benötigen keinerlei Therapie.
Die Ursachen einer angeborenen CMI sind noch nicht gänzlich geklärt. Zur Entstehung der CMI gibt es mehrere Theorien. Jedoch vermag bislang keine alle Erscheinungsbilder abzudecken. Eine der Theorien führt das Auftreten einer angeborenen CMI auf eine Veränderung im Erbgut (Mutation) während der Entwicklung des Nervensystems zurück. Diese spontane Mutation würde die korrekte Weiterentwicklung stören. Eine Vererbung wird nicht beobachtet.
Eine weitere Theorie führt die Entstehung einer CMI auf die engen Platzverhältnisse in der hinteren Schädelgrube (hinterer Bereich des Kopfes) zurück, die während der Entwicklung des Nervensystems vorliegen. Die Enge könne dazu führen, dass die dortigen Gehirnstrukturen durch die Öffnung gequetscht werden, die das Rückenmark und den Schädel verbindet (Foramen magnum).
Zu einer CMI können zudem gewisse Krankheitsbilder führen. Man spricht dann von einer sekundären CMI. Hirntumore, Hydrocephalus (Wasserkopf), Liquorverlustsyndrom (spontaner Verlust von Hirnwasser, typischerweise im Bereich vom Rücken nach einer Lumbalpunktion) und Anhaften des Rückenmarks an die umliegenden Strukturen (sogenanntes Tethered cord) können alle sekundär zu einer CMI führen. In solchen Fällen sollte die Ursache zuerst behandelt werden. Eine CMI kann ebenfalls gehäuft in Kombination mit gewissen Syndromen auftreten (Robin Sequenz, Neurofibromatose I Typ Recklinghausen und Noonan Syndrom).
Was ist eine Syringomyelie?
Eine Syringomyelie beschreibt einen flüssigkeitsgefüllten Hohlraum innerhalb des Rückenmarks und tritt oftmals zusammen mit einer CMI auf. Sie kann aber auch durch andere Ursachen bedingt sein: infektiös, entzündlich, traumatisch oder durch einen Hydrocephalus (Wasserkopf) oder eine Raumforderung (z.B. Tumor). Die Syringomyelie im Rahmen einer CMI kommt wahrscheinlich zustande, wenn die CMI zu einem erhöhten Druck im Gehirn führt und daraufhin Hirnwasser in das Rückenmark austritt. Dieser Druck baut sich auf, wenn der Rückfluss des Hirnwassers in den Schädel am Übergang zwischen Rückenmark und Gehirn blockiert ist. Mit der Zeit wird die angesammelte Flüssigkeit in das umliegende Gewebe gepresst. Es kommt zu einer Schwellung des Gewebes (Ödem) und in der Folge weitet das Ödem das Rückenmark auf (sogenannte Syrinx oder Syringomyelie).
Symptome
Was sind typische Zeichen einer Chiari Malformationen Typ I (CMI)
Bei 90
Prozent der CMI-Fälle handelt es sich um «inzidentelle Chiari-Malformationen»,
d.h. es treten keine Symptome auf. In den symptomatischen Fällen sind die
typischen Zeichen Nackenschmerzen, die in den Hinterkopf ausstrahlen, sowie ein
Taubheitsgefühl in den Fingern und Zehenspitzen etwa beim Husten, Niesen oder bei
Anstrengung. Weitere, seltenere Symptome sind eine Verformung des Rückens
(Skoliose), das Auftreten eines Wasserkopfes (Hydrocephalus) und
Hirnnervenausfälle, die sich bemerkbar machen als Heiserkeit, Stummheit,
Schluckprobleme, wiederholtes Verschlucken, abnormale Augenbewegungen,
Muskelschwächen oder Schlafapnoe (Aussetzen der Spontanatmung während des
Schlafens).
Die Symptome können sowohl im Kleinkindalter, aber auch erst in der Jugend beziehungsweise im früheren Erwachsenalter in Erscheinung treten.
Was sind typische Zeichen einer Syringomyelie
Eine
Syringomyelie zeigt eine grosse Bandbreite an Symptomen. In manchen Fällen
treten gar keine Symptome auf. Es kann aber auch zu Schmerzen oder zum Ausfall
des Schmerzempfindens oder Temperaturempfindens kommen. Ebenfalls bemerkbar machen können sich
Gangunsicherheit, Probleme mit dem Wasserlösen oder Stuhlgang (Inkontinenz) und
muskuläre Schwächen in den Armen oder Beinen. Seltener kann eine
Syringomyelie zu Störungen der Atmung und zu Schluckproblemen führen.
Diagnose
Wie wird eine Chiari Malformationen Typ I (CMI) diagnostiziert?
Bei Verdacht auf eine CMI oder Syringomyelie wird eine Bildgebung mittels Magnetresonanztomographie (MRI) vom Kopf und der Wirbelsäule durchgeführt. Oft wird eine CMI oder Syringomyelie auch zufällig bei einer MRI des Kopfes festgestellt, doch sofern keine Symptome vorhanden sind, ist dieser Zufallsbefund nicht behandlungsbedürftig. Ebenfalls kann eine CMI bereits während der Schwangerschaft mit einem pränatalen Ultraschall festgestellt werden.
Falls eine CMI im MRI
diagnostiziert wird, sollten möglich Ursachen hierfür (Tumor, tethered cord,
Liquorverlusstsyndrom, Hydrocephalus etc.) ausgeschlossen werden. Dies kann man
mit einer MRI-Untersuchung der gesamten spinalen Achse (Wirbelsäule und Kopf)
machen. Bei einer symptomatischen CMI werden wir für Ihr Kind weitere
Untersuchungen bei unseren Kolleg*innen der Augenmedizin, Hals-Nasen-Ohren-Medizin,
Kinderneurologie und eventuell der Schlafmedizin veranlassen, um sicherzustellen,
dass die Symptome durch die CMI verursacht werden.
Wie wird eine Syringomyelie diagnostiziert?
Bei der Diagnose einer Syringomyelie müssen ebenfalls mögliche Ursachen mittels einer MRI-Untersuchung der gesamten spinalen Achse ausgeschlossen werden. Falls die Syringomyelie Symptome verursacht, werden wir Ihr Kind durch Kolleg*innen aus der Kinderneurologie und eventuell Kinderurologie und -nephrologen mitbeurteilen lassen, also von Spezialist*innen der Harnwege und Harntrakt sowie Nieren. Eventuell wird auch eine Ultraschalluntersuchung der Blase und/oder Niere notwendig sein.
Therapie
Wie lässt sich eine Chiari Malformationen Typ I (CMI) behandeln?
Eine zufällig entdeckte CMI bedarf in der Regel keiner Therapie. Dabei kann der Krankheitsverlauf klinisch sowie mittels MRI nach einem Jahr nachkontrolliert werden. Falls die Situation stabil ist, braucht es in der Regel keine Nachkontrollen mehr.
Bei CMI-typischen Symptomen wird die chirurgische Therapie empfohlen. Das Ziel der chirurgischen Therapie ist die Entlastung der Ektopie im Übergang zwischen Hirn und Rückenmark. Dafür wird ein Teil vom Schädelknochen beim Übergang vom Hinterkopf zum Nacken (sogenannte extradurale Foramen Magnum Dekompression) sowie die hinteren Anteile der obersten Wirbelkörper im Nacken (sogenannte Laminektomie) entfernt, um zusätzlichen Platz für das Gehirn und dem Hirnstamm zu schaffen. Allenfalls ist es zusätzlich notwendig, die Hirnhaut (Dura) zu eröffnen, gegebenenfalls sogar die Kleinhirntonsillen zu verkleinern oder zu entfernen, um noch mehr Platz zu schaffen. Dies wird als intradurale Foramen magnum Dekompression bezeichnet. Durch diese Operationen wird der Druck im Kopf reduziert.
Das Kind wird unter Narkose in Bauchlage operiert. Es wird ein Schnitt am hinteren Schädel und oberen Nacken beim Übergang zum Rückenmark gemacht und dort ein Zugang zum Übergang eröffnet. Anschliessend wird ein Loch an der Hinterkante des Schädels gemacht (Kraniotomie) und der Dornfortsatz des ersten Halswirbelkörpers entfernt. Dann wird je nach Bedarf noch die Hirnhaut eröffnet, um die engen Platzverhältnisse zu erweitern. Wenn die Hirnhaut eröffnet wird, wird ein sogenannter Durapatch eingenäht. Dabei handelt es sich um eine künstliche Hirnhaut, die an die Schnittränder der echten, eröffneten Hirnhaut angenäht wird und die Hirnhaut somit wieder abdichtet. Anschliessend wird die Haut wieder verschlossen. Die gesamte Operation dauert ca. 2 bis 3 Stunden. Komplikationen einer Foramen magnum Dekompression sind selten (ca. 6%) und beinhalten Nacken- und Kopfschmerzen sowie das Risiko eines Hirnwasserlecks und einer Pseudomeningocele (Ansammlung von Hirnwasser unter der Haut).
Wie lässt sich eine Syringomyelie behandeln?
Falls eine begleitende Syringomyelie vorhanden ist, kann diese durch die CMI-Operation ebenfalls behoben werden. Falls dies nicht der Fall sein sollte, besteht mit der Syringomyelie-Operation eine weitere Möglichkeit, die überschüssige Hirnflüssigkeit aus dem Rückenmark abzuführen. Dabei wird ein Abflussröhrchen (sogenannter «Syringo-Subarachnoidalen Shunt») in den Raum zwischen Rückenmark und Hirnhäute eingelegt (Subarachnoidalraum). Durch dieses Röhrchen kann die Flüssigkeit entweder in das Lungenfell abfliessen (sogenannter «Syringo-Pleuraler Shunt»)oder in den Bauchraum(sogenannter «Syringo-Peritonealer Shunt»).
Die Komplikationsrate einer Syringomyelie-Operation ist gering und tritt bei ca. 3-5% der Fälle auf. Komplikationen können durch Verletzungen des Rückenmarks auftreten, welche zu einem Ausfall der Temperatur- oder Gefühlsempfindung oder aber auch zu muskulären Ausfällen führen können. Ebenfalls kann es zu einem Leck im Abflussröhrchen kommen, durch welches Hirnwasser austritt. In seltenen Fällen kann das Abflussröhrchen auch verstopfen und eine erneute Syringomyelie auftreten, was eine weitere Operation notwendig macht.
Spitalaufenthalt
Wie läuft der Spitalaufenthalt meines Kindes ab?
Während des gesamten Spitalaufenthaltes wird Ihr Kind von unserem Team der pädiatrischen Neurochirurgie im UKBB betreut. Ihr Kind tritt einen Tag vor der Operation ein und wird durch unser Team nochmals untersucht. Am nächsten Tag wird Ihr Kind operiert und kommt anschliessend zur Überwachung auf die Intensivpflegestation.
Am Operationstag steht Ihnen eine Begleiterin vom Elternbegleitungsservice (BELOP) der Stiftung Pro UKBB zur Verfügung. Sie begleitet Sie, bis Ihr Kind eingeschlafen ist, und zeigt Ihnen, wo es wieder aufwachen wird. Zwischendurch hilft sie Ihnen, sich im Spital zurechtzufinden.
Sobald Ihr Kind keine engmaschige Überwachung mehr braucht, kommt es auf die kinderchirurgische Bettenstation (2. Stock, Station B). Während der gesamten Hospitalisation dürfen Sie bei Ihrem Kind sein und sich mit Fragen an das Team der pädiatrischen Neurochirurgie wenden, welches täglich zur Visite bei Ihnen und Ihrem Kind vorbeikommt. Sobald Ihr Kind sich von der Operation erholt hat, darf es wieder nach Hause.
Prognose
Welche Prognose haben eine behandelte Chiari Malformationen Typ I (CMI) und eine Syringomyelie?
Die Prognose der CMI ist schwer vorherzusagen und hängt von den Symptomen der Erkrankung ab. Manche Patient*innen zeigen nie Symptome, andere sind schwerstgradig eingeschränkt, und manche Patient*innen entwickeln erst sehr spät Beschwerden. Durch eine Operation kann bei ca. 80 Prozent der Patient*innen mit CMI eine Verbesserung der Symptome erreicht werden.
Ähnlich verhält es sich mit der Syringomyelie. Auch dort können die Symptome stark einschränkend oder nicht einschränkend sein und Patient*innen können sich nach einer Operation potentiell erholen. Je länger eine Syringomyelie besteht, desto geringer wird allerdings das Erholungspotential, da die Syringomyelie mehr Zeit hat, Schäden im Rückenmark anzurichten.
Literatur
Weiterführende Literatur
Soleman J, Roth J, Constantini S. Direct syrinx drainage in patients with Chiari I malformation. Child’s Nerv Syst ChNS Off J Int Soc Pediatr Neurosurg. 2019;35(10):1863-1868. doi:10.1007/s00381-019-04228-7
Soleman J, Roth J, Constantini S. Syringo-subarachnoid shunt: how I do it. Acta Neurochir (Wien). 2019;161(2):367-370. doi:10.1007/s00701-019-03810-x
Soleman J, Bartoli A, Korn A, Constantini S, Roth J. Treatment failure of syringomyelia associated with Chiari I malformation following foramen magnum decompression: how should we proceed? Neurosurg Rev. 2019;42(3):705-714. doi:10.1007/s10143-018-01066-0
Soleman J, Roth J, Bartoli A, Rosenthal D, Korn A, Constantini S. Syringo-Subarachnoid Shunt for the Treatment of Persistent Syringomyelia Following Decompression for Chiari Type I Malformation: Surgical Results. World Neurosurg. 2017;108:836-843.
Bartoli A, Soleman J, Berger A, et al. Treatment Options for Hydrocephalus Following Foramen Magnum Decompression for Chiari I Malformation: A Multicenter Study. Neurosurgery. 2020;86(4):500-508. doi:10.1093/neuros/nyz211doi:10.1016/j.wneu.2017.08.002
Weitere Themen
Notfälle
Beratungstelefon
für
Kinder- und Jugendnotfälle
0900 712 712 (3.23 CHF/Min., nur über private Festnetz- oder Handynummern)
0900 712 713 (3.23 CHF/Min., für Anrufe von Prepaid-Handys)
0800 444 333 (Abrechnung via Krankenkasse, für Business-Anschlüsse)
Notfall im Ausland
Bei Notfällen im Ausland rufen Sie die Notfallnummer Ihrer Kranken-kasse an. Diese finden Sie jeweils auf Ihrer Krankenkassenkarte.
Tox Info Suisse
(Gift- und Informationszentrum)
145
Kontakt
Universitäts-Kinderspital beider
Basel, Spitalstrasse 33
4056 Basel | CH
Tel. +41 61 704 12 12
Kontaktformular
Kontakt
Universitäts-Kinderspital beider
Basel, Spitalstrasse 33
4056 Basel | CH
Tel. +41 61 704 12 12
Kontaktformular
© UKBB, 2024